美国食品和药物管理局批准Vemlidy®新二代治疗慢性乙型肝炎病毒感染
特别提示:Vemlidy是一种每日治疗,与Viread相比,具有改善的肾脏和骨骼实验室安全参数,具有相似的功效。
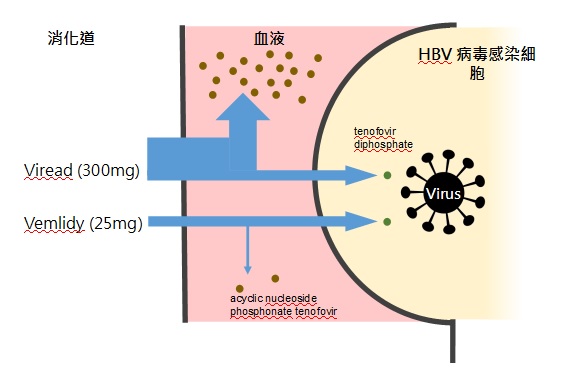
VEMLIDY 是一种新型的替诺福韦靶向前药,在临床研究中显示该药使用较小的剂量(25mg)便可达到跟替诺福韦(TDF,VIREAD® ,300mg)相似的临床效用。数据显示由于 VEMLIDY 相较于VIREAD® 拥有更大的血浆稳定性和更有效的将替诺福韦输送到肝细胞,因此该药使用剂量可以更低进而实现血流中替诺福韦含量可以更低。
因此,VEMLIDY 相较于 VIREAD® 肾功能和骨质安全性还可以获得改善。多伦多总医院肝病专家,多伦多大学医学助理教授Scott Fung博士表示“慢乙肝是一种威胁生命的疾病,需要长期甚至终身抗病毒治疗。但如今只有很少的可用抗病毒治疗药物可供选择,在某些患者中长期治疗后会出现一些不良反应。
临床研究已经显示 VEMLIDY 相较于 VIREAD® 可以更有效的抑制病毒,使转氨酶回复正常水平,并且肾功能和骨质安全性也获得改善。对许多慢乙肝患者来说这味新药意味着一种显著的进步。
多伦多总医院加拿大肝病基金会主席和肝病学家 Morris Sherman 博士说道,“慢乙肝通过治疗可以有效的获得控制,但患者必须终身用药。这种类型的延长治疗虽然保护了肝脏,但也会出现其他的健康并发症。医生必须拥有更多的治疗方案选择和降低剂量,提高安全性以满足患者的需求,进而实现在长期治疗期间患者会获得更好的临床结果。”
警告和注意事项
HBV / HIV-1合并感染患者HIV-1抗性发展的风险:由于这种风险,单独使用VEMLIDY不建议用于治疗HIV-1感染。尚未在HBV / HIV-1合并感染患者中建立VEMLIDY的安全性和有效性。在开始用VEMLIDY治疗之前,应该向所有HBV感染的患者提供HIV抗体检测,如果是阳性,应该使用推荐用于HBV / HIV-1合并感染患者的适当抗逆转录病毒联合治疗方案。
新发作或恶化的肾功能损害
使用替诺福韦前药报道了急性肾功能衰竭和范科尼综合征的病例。在VEMLIDY的临床试验中,没有Fanconi综合征或近端肾小管病变(PRT)的病例。肾功能受损和/或服用肾毒性药物(包括NSAIDs)的患者发生肾脏相关不良反应的风险增加。对于发生肾功能临床显着降低或Fanconi综合征证据的患者,停止使用VEMLIDY。
肾脏监测:在临床适当的所有患者开始和治疗期间评估血清肌酐,血清磷,CrCl,尿糖和尿蛋白。
不良反应
最常见的不良反应(发生率≥5%;所有年级)均为头痛,腹痛,乏力,咳嗽,恶心和背痛。
药物相互作用
VEMLIDY与降低肾功能或竞争活动性肾小管分泌的药物共同给药可能会增加替诺福韦的浓度和不良反应的风险。
不建议与以下药物共同使用VEMLIDY:奥卡西平,苯巴比妥,苯妥英,利福布汀,利福平,利福喷汀或圣约翰草。预计这种共同给药会降低替诺福韦艾拉酚胺的浓度,从而降低VEMLIDY的治疗效果。强烈影响P-gp和BCRP活性的药物可能导致VEMLIDY吸收的变化。
有关可能重要的药物相互作用(包括临床评论)的更多信息,请参阅VEMLIDY的完整处方信息。
剂量和给药
剂量:成人; 1片每日一次,每次一片。
价格:25毫克,30粒在美国的价格大约是1100美元。
肾功能损害:不建议CrCl <15 mL / min的患者使用。
肝功能损害:不推荐用于失代偿(Child-Pugh B或C)肝功能损害的患者。
在开始之前进行测试: HIV感染。

