美国药品标签上的五大”商“,生产商?经销商?包装商?标签商?持证商? 中国参比制剂一次性进口,要求提供药品的持证商和生产商的信息。因为中美药品法规的不同,几乎每一个办理参比进口的中国药企,都会遇到很难确认生产商信息的困境。本文从美国药品法规的角度,看看美国是如何来定义生产商?经销商?包装商?标签商?和持证商的? 并且,来回答一下,美国药品标签上(包括标签和说明书)上所列出的公司是哪个“商”,及其地址格式的要求。最后,讨论一下美国FDA是如何监管生产商cGMP车间地址信息的,和对中国参比制剂进口如何与国际接轨提出一些建议。
中国参比制剂一次性进口,要求提供药品的持证商和生产商的信息。因为中美药品法规的不同,几乎每一个办理参比进口的中国药企,都会遇到很难确认生产商信息的困境。本文从美国药品法规的角度,看看美国是如何来定义生产商?经销商?包装商?标签商?和持证商的? 并且,来回答一下,美国药品标签上(包括标签和说明书)上所列出的公司是哪个“商”,及其地址格式的要求。最后,讨论一下美国FDA是如何监管生产商cGMP车间地址信息的,和对中国参比制剂进口如何与国际接轨提出一些建议。
一,美国药品标签中的五大”商“的定义。
美国药品标签(包括说明书和药品上实际的标签)涉及五种功能的药企,一个药企可以同时承担这五大功能,同时是五大“商”。
A,生产商(MANUFACTURER)
联邦法规21CFR201.1中 (下面的截图),对生产商有非常明确的定义,包含了制剂生产企业的每一个步骤(见下面的英文描述)。 值得注意的是,这里面没有包括产品出厂分析检测和包装的步骤。生产商可以与其他四大”商“是同一家公司。
(b) As used in this section, and for purposes of section 502 (a) and (b)(1) of the act, the manufacturer of a drug product is the person who performs all of the following operations that are required to produce the product: (1) Mixing, (2) granulating, (3) milling, (4) molding, (5) lyophilizing, (6) tableting, (7) encapsulating, (8) coating, (9) sterilizing, and (10) filling sterile, aerosol, or gaseous drugs into dispensing containers.
参考文献衔接: https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfCFR/CFRSearch.cfm?fr=201.1 B,经销商(DISRTRIBUTOR)
B,经销商(DISRTRIBUTOR)
联邦法规21CFR201.1中也提到药品的经销商,在美国DITRIBUTOR的功能就是批发配送的意思,就是把药品从生产的厂家,绝大部分情况下是卖到大的批发商那里,少数情况下也可以直接卖给医院或者零售药房或者医生,但是,不能直接卖给病人的。 经销商可以与其他四大”商“是同一家公司。
(5) If the distributor is named on the label, the name shall be qualified by one of the following phrases: "Manufactured for ______", "Distributed by ______", "Manufactured by ______ for ______", "Manufactured for _____by _____", "Distributor: ______", "Marketed by ______". The qualifying phrases may be abbreviated.
C,包装商(PACKER)
联邦法规21CFR201.1中也提到药品的包装商。一般情况下,包装是做为生产的一部分,包装商就是生产商,包装商是不会单独列出来的。但是,美国存在一些独立的包装商,比如,他们把瓶子装的片剂,包装成铝塑的,或者把一大瓶口服的液体包装成5ML一杯的单剂量包装。包装商有自己独立的国家药品代码NDC。理论上包装商也可以和其他四大”商“是同一个公司,但是,在美国大多数的情况下,包装商不是生产商,也不是持证商。包装商经常是标签商,包装商可以是自己的经销商,也可以不是。
(6) If the packer is identified on the label, the name shall be qualified by the phrase "Packed by ______" or "Packaged by ______". The qualifying phrases may be abbreviated.
D,标签商(LABELER)
标签商就是美国国家药品代码的第一段数字所代表的公司,可以和其他四大”商“是同一家公司。
The FDA describes the National Drug Code (NDC) Number in the following way:
"Each listed drug product listed is assigned a unique 10-digit, 3-segment number. This number, known as the NDC, identifies the labeler, product, and trade package size. The first segment, the labeler code, is assigned by the FDA. A labeler is any firm that manufactures (including repackers or relabelers), or distributes (under its own name) the drug. The second segment, the product code, identifies a specific strength, dosage form, and formulation for a particular firm. The third segment, the package code, identifies package sizes and types. Both the product and package codes are assigned by the firm. The NDC will be in one of the following configurations: 4-4-2, 5-3-2, or 5-4-1."
E,持证商(APPLICANT HOLDER)
持证商是美国药品申请NDA或者ANDA的公司,就是橘皮书中APPLICANT HOLDER的公司。持证商可以与其他四大”商“是同一家公司。 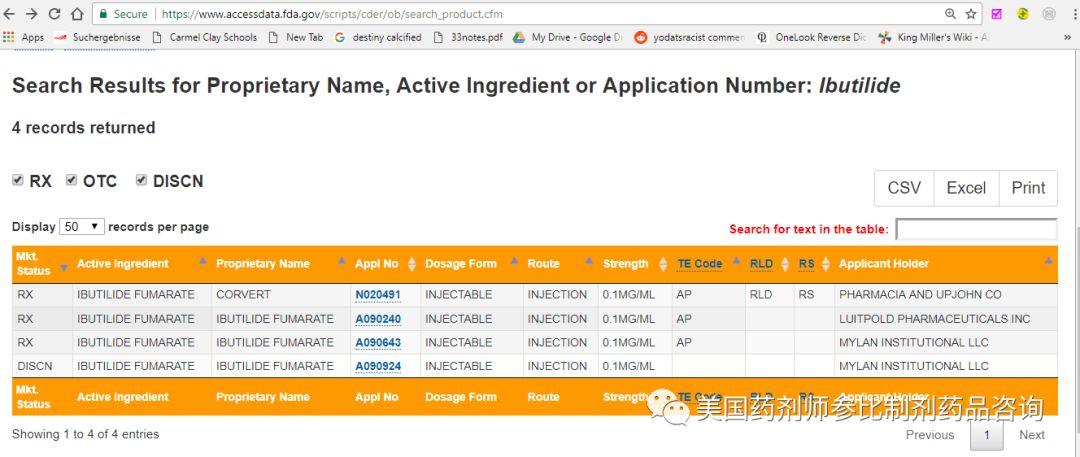 二,美国药品标签上列出的公司是哪个”商“?
二,美国药品标签上列出的公司是哪个”商“?
美国药品标签(包括药品说明书和贴的标签)需要注明哪个”商“?联邦法规21CFR201.1中明确规定如下,美国药品标签必须写明生产商,或者包装商,或者经销商。问题就是法律用词中的“或者”。美国药厂可以选择在药品的标签上显示三“商”之一,生产商或包装商或经销商。
(a) A drug or drug product (as defined in 320.1 of this chapter) in finished package form is misbranded under section 502 (a) and (b)(1) of the act if its label does not bear conspicuously the name and place of business of the manufacturer, packer, or distributor.
根据我们上面讨论的包装商的情况,包装商一般不适用于做参比制剂的大部分药品。所以,美国药厂必须在标签中提供二“商”之一,生产商或者经销商。因为生产商的信息比较复杂,比如辉瑞公司全球有很多生产商的地址,有的产品从几个不同的地址同时生产,生产商的地址经常改变,还有合同代加工生产商的情况,所以,在美国的药品标签上,提供具体cGMP生产商的地址不是很实际的做法。但是,美国联邦法律,允许生产商用总部的地址,代替具体cGMP车间的地址。
美国药品标签上,必须提供二“商”之一,生产商或者经销商。 原研公司希望宣传品牌效应,一般都会在标签上列出来经销商的信息,或者cGMP生产车间的总部的地址信息。对于原研新药来说,这二个“商”,经常都是同一个公司。但是,具体cGMP生产车间的地址,在美国的药品标签上,联邦法律不要求提供的。
中国药品一次性进口要求提供持证商和生产商的信息。从这里的分析可以看到,当药监老师拿着药品包装照片和说明书对照生产商和持证商的信息的时候,中国要求的二商(cGMP生产商+持证商)在美国药品的标签上,有可能,都找不到。幸运的是,美国的原研新药,大部分情况下,美国药品标签上所列出来的(”经销商“或者“生产商总部”)与中国要求的二”商“(”cGMP车间的生产商“+“持证商”),经常是同一家,药监老师从药品标签上,看到了所需要的“商”的名字也就让通过了。其实美国药品标签上写的“商”的名字,与国内进口批件上要求的二个“商”是不同的概念。
三,美国药品标签上,显示的“商”的公司地址的格式的要求。
因为中国一次性进口,必须提供二”商“的详细的地址,美国药品标签上“商”的地址,如果和一次性进口批件上的地址不一样,是100%无法通过的,必须重新办理批件或者退货,造成极大的资源和时间的浪费。我们来看看美国药品标签(包括说明书)上的地址的格式是怎么要求的。
联邦法规21CFR201.1中明确规定了“商”的地址的要求。法律首先指出,必须要提供街道,城市,州地址和邮编,但是,如果这个“商”在所在的城市里面的目录里或者电话目录里能查到(换句话说就是知名大公司),就不用提供街道地址了。但是,城市,州,邮编必须提供。这就是为什么我们看到的大部分的美国药品标签上显示的“商”的地址,只有城市,州和邮编的信息。美国办事,法律明确到每一个细节。中国一次性进口,现在也接受地址是“城市,州和邮编”的格式了,因为美国标签上是这么写的。但是,这样写地址的格式的法律来源,一般人不是很清楚的。
(i) The statement of the place of business shall include the street address, city, State, and ZIP Code. 。。。The street address may be omitted if it is shown in a current city directory or telephone directory. 。。。the ZIP Code shall appear either on the label or the labeling (including the invoice).
四,美国药品标签上,用制药公司总部的地址代替生产车间的地址。
关于生产商(cGMP车间)的地址,美国药品法明确的规定,药品标签上的“商”可以用总部的地址来代替具体生产车商(cGMP车间)的地址。中国一次性进口要求的生产商是具体的cGMP车间的地址。这样的要求,与美国法律不接轨,造成国内企业,像侦探一样,用尽各种方法,到处去寻找确认美国药品的cGMP生产车间的地址。
(j) If a person manufactures, packs, or distributes a drug or drug product at a place other than the person's principal place of business, the label may state the principal place of business in lieu of the actual place where such drug or drug product was manufactured or packed or is to be distributed, unless such statement would be misleading.
五,美国FDA如何监管的cGMP生产商信息?
美国FDA是通过持证商来监管生产车间地址的。持证商的新药证书里面(LICENSE),必须包含所有批准的cGMP生产车间的地址。 所有的药品生产车间信息(SITE)必须在NDA或者ANDA里面提供给FDA批准。以后再改生产地址,都需要FDA批准的(见下图FDA的指导文件)。每年每个生产车间所生产的批次等信息,都会在年度报告中,提供给FDA的,只是这样的信息,不对外公开的,中国药企在申请一次性进口的时候,无法获得某个药品的具体生产地址。

六,总结。
中国一次性进口的法规,最早来源于,跨国药企把他们在国外生产的药品进口到中国进行注册销售的流程和法规。跨国药企当然需要提供所有的生产商的信息和COA等。这样的法规来管理进口药品在中国注册销售是绝对没有问题的。其他亚洲国家也都是这样管理的。
只是把这样的法规,直接复制来管理一次性进口参比制剂药品,就完全是高射炮打蚊子。参比制剂,是一个特殊商品,国外药企是希望中国药企永远都不能进口参比制剂才好,这样中国永远没有仿制药来竞争原研药品。所以,国外药企是不会提供任何有帮助的信息的,比如COA。 国内药企只能根据公开发表的信息,来查找或者来猜测中国药监部门要求的提供的生产商的信息。
在中国一次性进口流程和法规开始以前,国内药企进口参比制剂,当时是要求药检所检验和提供COA。后来,随着一致性评价的开展,国内提出来一次性进口的流程,刚开始是要求提供国外原研公司的COA检验报告的,因为众多企业都无法提供COA,浪费了几个月的时间以后,药监部门认识到监管法规不合理,就把COA的要求去掉了。目前只剩下要求提供生产商的信息不合理了,这个一直困惑着国内药企,但是,一直到今天,这个不合理的法规还没有修改。
美国FDA对参比制剂,不要求合法来源的证明,不要求COO,没有任何多余的要求,只要提供包装盒子就可以了。 因为美国FDA知道,原研药企会千方百计的阻挠仿制药厂获得参比制剂,FDA在法规方面,给仿制药企业获得参比制剂大开绿灯,FDA没有任何不合理的多余的要求。中国药企在采购国外参比制剂的方面本来就处于不利的地位,加上中国药监部门人为的不合理的法规障碍。中国仿制药想要走出国门,中国想成为仿制药强国,在国际市场的竞争中取得一席之地,这些不合理的法规,虽然影响很小的一个方面,必须一点一点的进行改革。
张博士认为,中国监管参比制剂一次性进口,只需要提供持证商和来源国的信息,不需要提供生厂商的地址。 因为,生产商的地址信息,是美国法律不要求公开的,经常是查不到的。
另外,整个参比制剂一次性进口的流程管理方面,对比美国,欧洲,亚洲,以色列,中东国家的参比制剂药品一次性进口的流程法规,中国的还是流程太复杂,耗时太长,还是太高射炮打蚊子。希望能改革!希望能摒弃不合时宜的做法流程法规!我们已经看到国内医药方面推出很多令人振奋的改革之举,基本上都是向着国际上比较合理的做法靠近的,融合的。最后感慨一句,只有改革开放才能发展中国。
(原创)授权美国希望之光医疗,欢迎转载,请注明出处。 全球顶级医生协会(Global Top Doctors Association)是美国加州政府正式注册的联邦政府批准的一个非营利性,非宗教,非政治性国际社会组织,总部位于洛杉矶。全球顶级医生协会为中西方医学和精神专业人士的科学研究创造更有利的环境,为他们提供机会在社区,全国以及全球服务人群,满足民众的身体与精神健康需求。
全球顶级医生协会(Global Top Doctors Association)是美国加州政府正式注册的联邦政府批准的一个非营利性,非宗教,非政治性国际社会组织,总部位于洛杉矶。全球顶级医生协会为中西方医学和精神专业人士的科学研究创造更有利的环境,为他们提供机会在社区,全国以及全球服务人群,满足民众的身体与精神健康需求。

